নবম শ্রেণি: ভৌত বিজ্ঞান, অধ্যায় 4.1 : ‘পরমাণুর গঠন’ MCQ ও 1 নম্বরের প্রশ্নত্তোর
অধ্যায় ৪: পদার্থের পরমাণুর গঠন
(Structure of Atom)
ভূমিকা (Introduction)
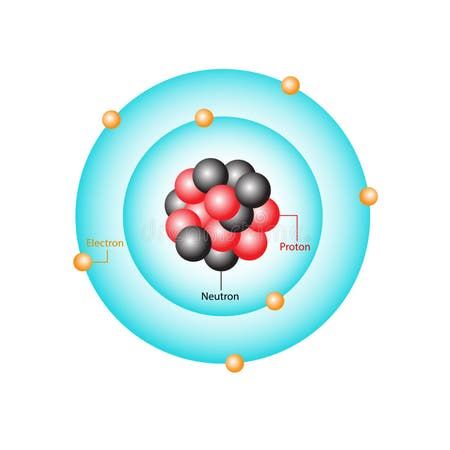
ডাল্টন বলেছিলেন পরমাণু অবিভাজ্য, অর্থাৎ একে আর ভাঙা যায় না। কিন্তু বিজ্ঞানের অগ্রগতির সাথে সাথে আমরা জানলাম পরমাণুর ভেতরেও এক বিশাল জগত লুকিয়ে আছে। সেখানে আছে ইলেকট্রন, প্রোটন আর নিউট্রন।
কীভাবে আবিষ্কৃত হলো এই কণাগুলো? পরমাণুর গঠন দেখতে কেমন? নিউক্লিয়াস কী? আইসোটোপ বা আইসোবার কাদের বলে? এই অধ্যায়ে আমরা পরমাণুর ভেতরের সেই রহস্যময় জগত সম্পর্কে জানব।
পরীক্ষায় সম্ভাব্য নম্বর বিভাজন (Probable Marks Distribution)
(দ্রষ্টব্য: স্কুলের বা বোর্ডের নিয়ম অনুযায়ী এই বিভাজন সামান্য পরিবর্তিত হতে পারে)
| প্রশ্নের ধরণ | প্রতি প্রশ্নের মান | মোট প্রশ্ন | মোট নম্বর |
|---|---|---|---|
| MCQ (বহুবিকল্পভিত্তিক) | 1 | 2 টি | 2 |
| VSAQ (অতি সংক্ষিপ্ত) | 1 | 3 টি | 3 |
| SAQ (সংক্ষিপ্ত) | 2 | 1 টি | 2 |
| LAQ (ব্যাখ্যামূলক) | 3 | 1 টি | 3 |
| সর্বমোট (Total Marks) | 10 নম্বর | ||
এই অধ্যায়ের মূল বিষয়বস্তু
- ⚛️ পরমাণুর মূল কণা: ইলেকট্রন, প্রোটন ও নিউট্রনের আবিষ্কার, আধান এবং ভরের তুলনা।
- 🔬 পরমাণু মডেল: রাদারফোর্ডের আলফা কণা বিচ্ছুরণ পরীক্ষা, নিউক্লিয়াস আবিষ্কার, বোর-এর পরমাণু মডেল ও তার স্বীকার্য।
- 🔢 পারমাণবিক সংখ্যা ও ভরসংখ্যা: প্রোটন সংখ্যা (Z), ভরসংখ্যা (A) এবং তাদের সম্পর্ক ($A = Z + N$)।
- 🔄 আইসোটোপ, আইসোবার ও আইসোটোন: সংজ্ঞা, উদাহরণ এবং আইসোটোপের ব্যবহার।
- 🪐 ইলেকট্রন বিন্যাস: কক্ষপথ বা শেল (K, L, M, N) ধারণা এবং $2n^2$ সূত্র অনুযায়ী ইলেকট্রন সজ্জা।
অধ্যায় ৪: পরমাণুর গঠন – MCQ
1. পরমাণু অবিভাজ্য (Indivisible)—এই মতবাদটি কার?
- (A) রাদারফোর্ড
- (B) ডাল্টন
- (C) বোর
- (D) থমসন
উত্তর দেখো
উত্তর: (B) ডাল্টন
2. ইলেকট্রন কে আবিষ্কার করেন?
- (A) জে. জে. থমসন
- (B) রাদারফোর্ড
- (C) স্যাডউইক
- (D) গোল্ডস্টাইন
উত্তর দেখো
উত্তর: (A) জে. জে. থমসন
3. পরমাণুর নিউক্লিয়াস কে আবিষ্কার করেন?
- (A) বোর
- (B) থমসন
- (C) রাদারফোর্ড
- (D) সমারফিল্ড
উত্তর দেখো
উত্তর: (C) রাদারফোর্ড
4. পরমাণুর সবচেয়ে হালকা কণা কোনটি?
- (A) প্রোটন
- (B) নিউট্রন
- (C) ইলেকট্রন
- (D) আলফা কণা
উত্তর দেখো
উত্তর: (C) ইলেকট্রন
5. নিউট্রন বিহীন একটি পরমাণুর নাম লেখো।
- (A) সাধারণ হাইড্রোজেন (প্রোটিয়াম)
- (B) ডয়টেরিয়াম
- (C) হিলিয়াম
- (D) লিথিয়াম
উত্তর দেখো
উত্তর: (A) সাধারণ হাইড্রোজেন (প্রোটিয়াম)
6. পরমাণুর নিস্তড়িৎ কণা কোনটি?
- (A) ইলেকট্রন
- (B) প্রোটন
- (C) নিউট্রন
- (D) পজিট্রন
উত্তর দেখো
উত্তর: (C) নিউট্রন
7. রাদারফোর্ডের পরীক্ষায় কোন ধাতুর পাত ব্যবহার করা হয়েছিল?
- (A) রূপো
- (B) তামা
- (C) সোনা
- (D) অ্যালুমিনিয়াম
উত্তর দেখো
উত্তর: (C) সোনা
8. পারমাণবিক সংখ্যা (Atomic Number) বলতে কী বোঝায়?
- (A) ইলেকট্রন সংখ্যা
- (B) প্রোটন সংখ্যা
- (C) নিউট্রন সংখ্যা
- (D) নিউক্লিয়ন সংখ্যা
উত্তর দেখো
উত্তর: (B) প্রোটন সংখ্যা
9. ভরসংখ্যা (Mass Number) হলো—
- (A) প্রোটন + ইলেকট্রন
- (B) নিউট্রন + ইলেকট্রন
- (C) প্রোটন + নিউট্রন
- (D) কেবল নিউট্রন
উত্তর দেখো
উত্তর: (C) প্রোটন + নিউট্রন
10. আলফা কণা (Alpha particle) আসলে কী?
- (A) একটি প্রোটন
- (B) একটি ইলেকট্রন
- (C) দ্বি-পজিটিভ হিলিয়াম আয়ন ($He^{2+}$)
- (D) হাইড্রোজেন আয়ন
উত্তর দেখো
উত্তর: (C) দ্বি-পজিটিভ হিলিয়াম আয়ন ($He^{2+}$)
11. কোনো কক্ষপথে সর্বোচ্চ ইলেকট্রন ধারণ ক্ষমতা নির্ণয়ের সূত্র কোনটি?
- (A) $n^2$
- (B) $2n^2$
- (C) $2n+1$
- (D) $n$
উত্তর দেখো
উত্তর: (B) $2n^2$
12. M কক্ষে (n=3) সর্বোচ্চ কয়টি ইলেকট্রন থাকতে পারে?
- (A) 8
- (B) 18
- (C) 32
- (D) 2
উত্তর দেখো
উত্তর: (B) 18 (সূত্র: $2 \times 3^2 = 18$)
13. ‘প্লাডিং পুডিং’ (Plum Pudding) মডেল কার দেওয়া?
- (A) রাদারফোর্ড
- (B) বোর
- (C) থমসন
- (D) স্যাডউইক
উত্তর দেখো
উত্তর: (C) থমসন
14. পরমাণুর ভরের অধিকাংশ কোথায় থাকে?
- (A) ইলেকট্রনে
- (B) কক্ষপথে
- (C) নিউক্লিয়াসে
- (D) সমগ্র আয়তন জুড়ে
উত্তর দেখো
উত্তর: (C) নিউক্লিয়াসে
15. $_{17}^{35}Cl$ পরমাণুতে নিউট্রন সংখ্যা কত?
- (A) 17
- (B) 35
- (C) 18
- (D) 52
উত্তর দেখো
উত্তর: (C) 18 ($35 – 17 = 18$)
16. নিউট্রন কে আবিষ্কার করেন?
- (A) রাদারফোর্ড
- (B) স্যাডউইক (Chadwick)
- (C) বোর
- (D) গোল্ডস্টাইন
উত্তর দেখো
উত্তর: (B) স্যাডউইক (Chadwick)
17. আইসোটোপগুলির মধ্যে কোন কণার সংখ্যা সমান থাকে?
- (A) নিউট্রন
- (B) প্রোটন
- (C) ভরসংখ্যা
- (D) পজিট্রন
উত্তর দেখো
উত্তর: (B) প্রোটন
18. আইসোবারগুলির (Isobar) মধ্যে কোনটি সমান থাকে?
- (A) ইলেকট্রন সংখ্যা
- (B) প্রোটন সংখ্যা
- (C) ভরসংখ্যা
- (D) নিউট্রন সংখ্যা
উত্তর দেখো
উত্তর: (C) ভরসংখ্যা
19. সোডিয়ামের (Na, পারমাণবিক সংখ্যা ১১) ইলেকট্রন বিন্যাস কোনটি?
- (A) 2, 9
- (B) 2, 8, 1
- (C) 2, 7, 2
- (D) 2, 8
উত্তর দেখো
উত্তর: (B) 2, 8, 1
20. যে মৌলের পরমাণু ক্রমাঙ্ক ৬, তার যোজ্যতা ইলেকট্রন সংখ্যা কত?
- (A) ২
- (B) ৪
- (C) ৬
- (D) ১
উত্তর দেখো
উত্তর: (B) ৪ (বিন্যাস: ২, ৪)
21. তেজস্ক্রিয় আইসোটোপ C-14 কী কাজে ব্যবহৃত হয়?
- (A) ক্যানসার চিকিৎসায়
- (B) জীবাশ্মের বয়স নির্ণয়ে
- (C) থাইরয়েডের চিকিৎসায়
- (D) বিদ্যুৎ উৎপাদনে
উত্তর দেখো
উত্তর: (B) জীবাশ্মের বয়স নির্ণয়ে (Carbon Dating)
22. নিউক্লিয়াসের স্থায়িত্বের জন্য দায়ী বল কোনটি?
- (A) মহাকর্ষ বল
- (B) স্থির-তাড়িতিক বল
- (C) নিউক্লীয় বল
- (D) চৌম্বক বল
উত্তর দেখো
উত্তর: (C) নিউক্লীয় বল
23. $^{30}Si_{14}$ এবং $^{31}P_{15}$ হলো পরস্পরের—
- (A) আইসোটোপ
- (B) আইসোবার
- (C) আইসোটোন
- (D) আইসোমার
উত্তর দেখো
উত্তর: (C) আইসোটোন (উভয়ের নিউট্রন সংখ্যা ১৬)
24. পরমাণুর ব্যাস নিউক্লিয়াসের ব্যাসের প্রায় কত গুণ?
- (A) ১০ গুণ
- (B) ১০০ গুণ
- (C) ১০,০০০ গুণ
- (D) ১,০০,০০০ গুণ
উত্তর দেখো
উত্তর: (D) ১,০০,০০০ গুণ (প্রায়)
25. পরমাণুর নিউক্লিয়াসে কোন আধান থাকে?
- (A) ধনাত্মক
- (B) ঋণাত্মক
- (C) নিস্তড়িৎ
- (D) কোনোটিই নয়
উত্তর দেখো
উত্তর: (A) ধনাত্মক (প্রোটনের জন্য)
26. $Cl^-$ আয়নে ইলেকট্রন সংখ্যা কত? (Cl এর পারমাণবিক সংখ্যা ১৭)
- (A) ১৭
- (B) ১৬
- (C) ১৮
- (D) ৩৫
উত্তর দেখো
উত্তর: (C) ১৮ ($১৭+১=১৮$)
27. সাধারণ অবস্থায় পরমাণু তড়িৎ—
- (A) ধনাত্মক
- (B) ঋণাত্মক
- (C) নিরপেক্ষ
- (D) সুপরিবাহী
উত্তর দেখো
উত্তর: (C) নিরপেক্ষ (ইলেকট্রন = প্রোটন)
28. কোন আইসোটোপটি গলগন্ড (Goitre) চিকিৎসায় ব্যবহৃত হয়?
- (A) কোবাল্ট-৬০
- (B) আয়োডিন-১৩১
- (C) কার্বন-১৪
- (D) সোডিয়াম-২৪
উত্তর দেখো
উত্তর: (B) আয়োডিন-১৩১
29. পরমাণুর রাসায়নিক ধর্ম নির্ভর করে মূলত—
- (A) নিউট্রন সংখ্যার ওপর
- (B) ভরসংখ্যার ওপর
- (C) ইলেকট্রন বিন্যাসের ওপর
- (D) নিউক্লিয়াসের আকারের ওপর
উত্তর দেখো
উত্তর: (C) ইলেকট্রন বিন্যাসের ওপর
30. হাইড্রোজেনের কোন আইসোটোপে ১টি প্রোটন ও ১টি নিউট্রন আছে?
- (A) প্রোটিয়াম
- (B) ডয়টেরিয়াম
- (C) ট্রিটিয়াম
- (D) কোনোটিই নয়
উত্তর দেখো
উত্তর: (B) ডয়টেরিয়াম
অধ্যায় ৪: পরমাণুর গঠন – সত্য/মিথ্যা যাচাই
1. পরমাণুর নিউক্লিয়াস সর্বদা ধনাত্মক আধানযুক্ত হয়।
উত্তর দেখো
উত্তর: সত্য (প্রোটনের উপস্থিতির জন্য)।
2. ডাল্টনের মতে পরমাণু অবিভাজ্য।
উত্তর দেখো
উত্তর: সত্য (যদিও আধুনিক বিজ্ঞানে এটি ভুল প্রমাণিত হয়েছে, কিন্তু ডাল্টনের মতবাদ অনুযায়ী এটি সত্য ছিল)।
3. ইলেকট্রন হলো পরমাণুর সবচেয়ে ভারী কণা।
উত্তর দেখো
উত্তর: মিথ্যা (সবচেয়ে হালকা কণা)।
4. আইসোটোপগুলির পারমাণবিক সংখ্যা একই থাকে।
উত্তর দেখো
উত্তর: সত্য।
5. ক্যাথোড রশ্মি ঋণাত্মক আধানযুক্ত কণার স্রোত।
উত্তর দেখো
উত্তর: সত্য (ইলেকট্রনের স্রোত)।
6. রাদারফোর্ড আলফা কণা বিচ্ছুরণ পরীক্ষায় সোনার পাত ব্যবহার করেছিলেন।
উত্তর দেখো
উত্তর: সত্য।
7. পরমাণুর ভরসংখ্যা সর্বদা পূর্ণসংখ্যা হয়।
উত্তর দেখো
উত্তর: সত্য (প্রোটন ও নিউট্রন সংখ্যার যোগফল সর্বদা পূর্ণসংখ্যা)।
8. নিউট্রন একটি ধনাত্মক আধানযুক্ত কণা।
উত্তর দেখো
উত্তর: মিথ্যা (নিউট্রন নিস্তড়িৎ কণা)।
9. M কক্ষে সর্বোচ্চ ১৮টি ইলেকট্রন থাকতে পারে।
উত্তর দেখো
উত্তর: সত্য ($2n^2 = 2 \times 3^2 = 18$)।
10. সাধারণ হাইড্রোজেনে (প্রোটিয়াম) কোনো নিউট্রন নেই।
উত্তর দেখো
উত্তর: সত্য।
11. $^{40}Ar_{18}$ এবং $^{40}Ca_{20}$ হলো পরস্পরের আইসোটোপ।
উত্তর দেখো
উত্তর: মিথ্যা (এরা আইসোবার, কারণ ভরসংখ্যা সমান)।
12. পরমাণুর নিউক্লিয়াসের ঘনত্ব খুব কম।
উত্তর দেখো
উত্তর: মিথ্যা (নিউক্লিয়াসের ঘনত্ব অত্যন্ত বেশি)।
13. আলফা কণা হলো হিলিয়াম পরমাণুর নিউক্লিয়াস।
উত্তর দেখো
উত্তর: সত্য (দ্বি-পজিটিভ হিলিয়াম আয়ন)।
14. বোর-এর মডেল অনুযায়ী ইলেকট্রন নিউক্লিয়াসের চারদিকে বৃত্তাকার পথে ঘোরে।
উত্তর দেখো
উত্তর: সত্য।
15. পরমাণুর রাসায়নিক ধর্ম তার প্রোটন সংখ্যার ওপর নির্ভর করে।
উত্তর দেখো
উত্তর: সত্য (ইলেকট্রন বিন্যাস প্রোটন সংখ্যার ওপর নির্ভরশীল)।
16. নিউট্রন আবিষ্কার করেন বিজ্ঞানী স্যাডউইক।
উত্তর দেখো
উত্তর: সত্য।
17. $^{14}C$ একটি তেজস্ক্রিয় আইসোটোপ।
উত্তর দেখো
উত্তর: সত্য।
18. একটি প্রোটনের ভর একটি ইলেকট্রনের ভরের প্রায় সমান।
উত্তর দেখো
উত্তর: মিথ্যা (প্রোটন প্রায় ১৮৩৭ গুণ ভারী)।
19. পরমাণুর সবচেয়ে বাইরের কক্ষে সর্বোচ্চ ৮টির বেশি ইলেকট্রন থাকতে পারে না।
উত্তর দেখো
উত্তর: সত্য (অষ্টক সূত্রানুযায়ী)।
20. অ্যানোড রশ্মি ইলেকট্রন কণার স্রোত।
উত্তর দেখো
উত্তর: মিথ্যা (অ্যানোড রশ্মি ধনাত্মক আধানযুক্ত কণার স্রোত)।
21. $Na^+$ আয়নে মোট ১০টি ইলেকট্রন আছে।
উত্তর দেখো
উত্তর: সত্য ($11 – 1 = 10$)।
22. পারমাণবিক সংখ্যাকে Z অক্ষর দ্বারা প্রকাশ করা হয়।
উত্তর দেখো
উত্তর: সত্য।
23. নিউক্লীয় বল মহাকর্ষ বলের চেয়ে দুর্বল।
উত্তর দেখো
উত্তর: মিথ্যা (নিউক্লীয় বল প্রকৃতির সবচেয়ে শক্তিশালী বল)।
24. ভরসংখ্যা (A) = পারমাণবিক সংখ্যা (Z) + নিউট্রন সংখ্যা (N)।
উত্তর দেখো
উত্তর: সত্য।
অধ্যায় ৪: পরমাণুর গঠন – শূন্যস্থান পূরণ (পর্ব-১)
1. ইলেকট্রন আবিষ্কার করেন বিজ্ঞানী ________।
উত্তর দেখো
উত্তর: জে. জে. থমসন
2. পরমাণুর নিউক্লিয়াস আবিষ্কার করেন বিজ্ঞানী ________।
উত্তর দেখো
উত্তর: রাদারফোর্ড
3. নিউট্রন হলো একটি ________ কণা।
উত্তর দেখো
উত্তর: নিস্তড়িৎ (আধানহীন)
4. পরমাণুর সবচেয়ে হালকা কণা হলো ________।
উত্তর দেখো
উত্তর: ইলেকট্রন
5. আলফা কণা হলো মূলত দ্বি-পজিটিভ ________ আয়ন।
উত্তর দেখো
উত্তর: হিলিয়াম ($He^{2+}$)
6. পরমাণুর ভরের প্রায় সবটুকুই থাকে তার ________ -এ।
উত্তর দেখো
উত্তর: নিউক্লিয়াস (কেন্দ্রে)
7. বোর-এর মডেল অনুযায়ী ইলেকট্রন নিউক্লিয়াসের চারদিকে ________ পথে ঘোরে।
উত্তর দেখো
উত্তর: বৃত্তাকার
8. পরমাণুর ‘প্লাডিং পুডিং’ মডেলের প্রবক্তা ছিলেন ________।
উত্তর দেখো
উত্তর: জে. জে. থমসন
9. পরমাণুর নিউক্লিয়াসের ব্যাস পরমাণুর ব্যাসের প্রায় ________ ভাগ।
উত্তর দেখো
উত্তর: ১ লক্ষ (১/১০০০০০)
10. সাধারণ অবস্থায় পরমাণু তড়িৎ ________।
উত্তর দেখো
উত্তর: নিরপেক্ষ (Neutral)
11. প্রোটনের আধান ________।
উত্তর দেখো
উত্তর: ধনাত্মক
12. কোনো কক্ষপথে ইলেকট্রন ধারণ ক্ষমতা নির্ণয়ের সূত্রটি হলো ________।
উত্তর দেখো
উত্তর: $2n^2$
13. K কক্ষে সর্বোচ্চ ________ টি ইলেকট্রন থাকতে পারে।
উত্তর দেখো
উত্তর: ২
14. পারমাণবিক সংখ্যাকে ________ অক্ষর দ্বারা প্রকাশ করা হয়।
উত্তর দেখো
উত্তর: Z
15. ভরসংখ্যাকে ________ অক্ষর দ্বারা প্রকাশ করা হয়।
উত্তর দেখো
উত্তর: A
16. আইসোটোপগুলির ________ সংখ্যা সমান থাকে।
উত্তর দেখো
উত্তর: প্রোটন (বা পারমাণবিক)
17. আইসোবারগুলির ________ সংখ্যা সমান থাকে।
উত্তর দেখো
উত্তর: ভর
18. আইসোটোনগুলির ________ সংখ্যা সমান থাকে।
উত্তর দেখো
উত্তর: নিউট্রন
19. হাইড্রোজেনের ________ আইসোটোপে কোনো নিউট্রন নেই।
উত্তর দেখো
উত্তর: প্রোটিয়াম (সাধারণ হাইড্রোজেন)
20. কার্বন-১৪ আইসোটোপটি ________ নির্ণয়ে ব্যবহৃত হয়।
উত্তর দেখো
উত্তর: জীবাশ্মের বয়স
21. আয়োডিন-১৩১ আইসোটোপটি ________ রোগের চিকিৎসায় ব্যবহৃত হয়।
উত্তর দেখো
উত্তর: গলগন্ড (Goitre)
22. সোডিয়াম (Na)-এর ইলেকট্রন বিন্যাস হলো ________।
উত্তর দেখো
উত্তর: 2, 8, 1
23. নিউক্লিয়াসের স্থায়িত্বের জন্য দায়ী বল হলো ________ বল।
উত্তর দেখো
উত্তর: নিউক্লীয়
24. পরমাণুর সবচেয়ে বাইরের কক্ষে সর্বোচ্চ ________ টি ইলেকট্রন থাকতে পারে।
উত্তর দেখো
উত্তর: ৮
25. $_{18}^{40}Ar$ এবং $_{20}^{40}Ca$ হলো পরস্পরের ________।
উত্তর দেখো
উত্তর: আইসোবার
26. ভরসংখ্যা = প্রোটন সংখ্যা + ________ সংখ্যা।
উত্তর দেখো
উত্তর: নিউট্রন
অধ্যায় ৪: পরমাণুর গঠন – অতি সংক্ষিপ্ত প্রশ্ন
1. ইলেকট্রন কে আবিষ্কার করেন?
উত্তর দেখো
উত্তর: জে. জে. থমসন (J.J. Thomson)।
2. পরমাণুর নিউক্লিয়াস কে আবিষ্কার করেন?
উত্তর দেখো
উত্তর: আর্নেস্ট রাদারফোর্ড।
3. পরমাণুর নিস্তড়িৎ কণাটির নাম কী?
উত্তর দেখো
উত্তর: নিউট্রন।
4. প্রোটনের আধান বা চার্জ কী প্রকৃতির?
উত্তর দেখো
উত্তর: ধনাত্মক (Positive)।
5. পরমাণুর তিনটি মূল কণার মধ্যে সবচেয়ে হালকা কোনটি?
উত্তর দেখো
উত্তর: ইলেকট্রন।
6. হাইড্রোজেনের কোন আইসোটোপে কোনো নিউট্রন নেই?
উত্তর দেখো
উত্তর: প্রোটিয়াম বা সাধারণ হাইড্রোজেন ($^1_1H$)।
7. K কক্ষে (১ম কক্ষে) সর্বোচ্চ কয়টি ইলেকট্রন থাকতে পারে?
উত্তর দেখো
উত্তর: ২ টি।
8. কোনো কক্ষপথে ইলেকট্রন ধারণ ক্ষমতা নির্ণয়ের সাধারণ সূত্রটি কী?
উত্তর দেখো
উত্তর: $2n^2$ (যেখানে n = কক্ষপথের ক্রমিক সংখ্যা)।
9. নিউট্রন কে আবিষ্কার করেন?
উত্তর দেখো
উত্তর: জেমস স্যাডউইক (James Chadwick)।
10. আলফা কণা (Alpha Particle) আসলে কী?
উত্তর দেখো
উত্তর: দ্বি-পজিটিভ হিলিয়াম আয়ন বা হিলিয়াম নিউক্লিয়াস ($He^{2+}$)।
11. ভরসংখ্যা (A), পারমাণবিক সংখ্যা (Z) ও নিউট্রন সংখ্যা (N)-এর মধ্যে সম্পর্ক কী?
উত্তর দেখো
উত্তর: $A = Z + N$ বা $N = A – Z$।
12. কার্বনের (পারমাণবিক সংখ্যা ৬) ইলেকট্রন বিন্যাস লেখো।
উত্তর দেখো
উত্তর: K(2), L(4) বা ২, ৪।
13. কোন বলের প্রভাবে নিউক্লিয়াসের মধ্যে প্রোটন ও নিউট্রনগুলি একসঙ্গে থাকে?
উত্তর দেখো
উত্তর: নিউক্লীয় বল (Nuclear Force)।
14. পরমাণুর আকারের তুলনায় নিউক্লিয়াসের আকার কেমন?
উত্তর দেখো
উত্তর: অত্যন্ত ক্ষুদ্র (প্রায় ১ লক্ষ ভাগের ১ ভাগ)।
15. আইসোবার (Isobar) কাদের বলে?
উত্তর দেখো
উত্তর: ভিন্ন মৌলের যেসব পরমাণুর ভরসংখ্যা সমান কিন্তু পারমাণবিক সংখ্যা ভিন্ন, তাদের আইসোবার বলে।
16. ক্যানসার চিকিৎসায় ব্যবহৃত হয় এমন একটি আইসোটোপের নাম লেখো।
উত্তর দেখো
উত্তর: কোবাল্ট-৬০ (Co-60)।
17. পারমাণবিক সংখ্যা বা পরমাণু ক্রমাঙ্ক কাকে বলে?
উত্তর দেখো
উত্তর: কোনো মৌলের নিউক্লিয়াসে উপস্থিত মোট প্রোটন সংখ্যাকে ওই মৌলের পারমাণবিক সংখ্যা বলে।
18. নিউক্লিয়াসের আধান কী প্রকৃতির?
উত্তর দেখো
উত্তর: ধনাত্মক (Positive) প্রকৃতির।
19. একটি প্রোটন একটি ইলেকট্রনের চেয়ে প্রায় কত গুণ ভারী?
উত্তর দেখো
উত্তর: প্রায় ১৮৩৭ গুণ।
20. কোন পরমাণু মডেলকে ‘সৌর মডেল’ (Solar Model) বলা হয়?
উত্তর দেখো
উত্তর: রাদারফোর্ডের পরমাণু মডেলকে।
21. যোজ্যতা কক্ষ (Valence Shell) কাকে বলে?
উত্তর দেখো
উত্তর: পরমাণুর সবচেয়ে বাইরের কক্ষপথকে যোজ্যতা কক্ষ বলে।
22. পরমাণুর সবচেয়ে বাইরের কক্ষে সর্বোচ্চ কয়টি ইলেকট্রন থাকতে পারে?
উত্তর দেখো
উত্তর: ৮ টি।
23. আইসোটোন (Isotone) কাকে বলে?
উত্তর দেখো
উত্তর: ভিন্ন মৌলের যেসব পরমাণুর নিউট্রন সংখ্যা সমান, তাদের আইসোটোন বলে।
24. একটি তেজস্ক্রিয় আইসোটোপের নাম লেখো।
উত্তর দেখো
উত্তর: কার্বন-১৪ ($C^{14}$) বা ইউরেনিয়াম-২৩৫ ($U^{235}$)।
25. ক্লোরিনের (পারমাণবিক সংখ্যা ১৭) ইলেকট্রন বিন্যাস লেখো।
উত্তর দেখো
উত্তর: ২, ৮, ৭।
26. পরমাণুর কোন কণা তার রাসায়নিক ধর্ম নিয়ন্ত্রণ করে?
উত্তর দেখো
উত্তর: ইলেকট্রন (বিশেষ করে যোজ্যতা ইলেকট্রন)।
27. পরমাণুতে ‘সুস্থিত কক্ষপথ’ (Stationary Orbit)-এর ধারণা কে দেন?
উত্তর দেখো
উত্তর: নীলস বোর (Niels Bohr)।
28. অ্যানোড রশ্মি বা ক্যানাল রশ্মি কোন আধানযুক্ত?
উত্তর দেখো
উত্তর: ধনাত্মক আধানযুক্ত।
29. হিলিয়াম পরমাণুতে ($^4_2He$) কয়টি নিউট্রন আছে?
উত্তর দেখো
উত্তর: ২ টি ($4 – 2 = 2$)।
30. প্রোটিয়াম বা সাধারণ হাইড্রোজেনের ভরসংখ্যা কত?
উত্তর দেখো
উত্তর: ১ (১টি প্রোটন + ০টি নিউট্রন)।
31. ‘Atom’ শব্দটির অর্থ কী?
উত্তর দেখো
উত্তর: অবিভাজ্য (Indivisible)।
32. সাধারণ অবস্থায় পরমাণু তড়িৎ নিরপেক্ষ হয় কেন?
উত্তর দেখো
উত্তর: কারণ পরমাণুতে মোট প্রোটন সংখ্যা ও মোট ইলেকট্রন সংখ্যা সমান থাকে।
33. L কক্ষে সর্বোচ্চ কয়টি ইলেকট্রন থাকতে পারে?
উত্তর দেখো
উত্তর: ৮ টি ($2 \times 2^2 = 8$)।
34. পরমাণুর ভর মূলত কাদের ভরের যোগফল?
উত্তর দেখো
উত্তর: প্রোটন ও নিউট্রনের ভর (ইলেকট্রনের ভর নগণ্য)।
35. যোজ্যতার সংজ্ঞা দাও।
উত্তর দেখো
উত্তর: কোনো মৌলের অন্য মৌলের সাথে যুক্ত হওয়ার ক্ষমতাকে (সাধারণত হাইড্রোজেন পরমাণুর সংখ্যার নিরিখে) যোজ্যতা বলে।
36. ক্যাটায়ন সৃষ্টি হয় ইলেকট্রন বর্জনের ফলে না গ্রহণের ফলে?
উত্তর দেখো
উত্তর: ইলেকট্রন বর্জনের ফলে (ধনাত্মক আধান যুক্ত হয়)।
